“頭對頭”試驗!艾貝格司亭α長效升白再添新證
3月14日,正大天晴艾貝格司亭α(商品名:億立舒)的一項“頭對頭”全球Ⅲ期研究(GC-627-05)數據發表于國際期刊《JCO Oncology Advances》。研究結果顯示,艾貝格司亭α在預防化療引起的中性粒細胞減少癥(CIN)的臨床試驗中,非劣效于培非格司亭,且在后續化療周期中表現出更低的嚴重中性粒細胞減少發生率[1]。

給化療系上“安全帶”
化療引起的中性粒細胞減少(CIN)是癌癥患者接受骨髓抑制性化療時常見的劑量限制性毒性反應。中性粒細胞減少不僅會增加感染風險,還可能導致化療劑量減少或治療延遲,嚴重時甚至危及患者生命。為了預防CIN,粒細胞集落刺激因子(G-CSF)類藥物被廣泛使用,尤其是長效G-CSF,如培非格司亭。
艾貝格司亭α是全球首個第三代長效G-CSF-Fc融合蛋白。已有研究證實,艾貝格司亭α在預防CIN方面的療效和安全性與短效G-CSF非格司亭相當[2,3]。本研究旨在進一步評估艾貝格司亭α在乳腺癌患者中的有效性和安全性,特別是在多周期化療中的表現。
本研究為全球多中心、隨機、開放標簽、陽性對照的非劣效Ⅲ期臨床試驗,在5個國家的41個研究中心進行。研究共納入393例接受化療(多西他賽+環磷酰胺)的Ⅰ-Ⅲ期乳腺癌患者,受試者按1:1的比例隨機分配至艾貝格司亭α組或培非格司亭組。
長效預防潛力添新證
研究結果顯示,主要終點艾貝格司亭α組和培非格司亭組在第一個化療周期內,4級中性粒細胞減少(ANC<0.5×109/L)的持續時間分別為0.2±0.51天和0.2±0.45天(95% CI: -0.1, 0.1; P=0.7074),證實了艾貝格司亭α非劣效于培非格司亭[1]。在后續第三個和第四個化療周期中,艾貝格司亭α組的4級中性粒細胞減少發生率分別為2.6%和1.6%,培非格司亭組分別為6.3%和5.3%[1],艾貝格司亭α組多周期預防潛力突出。
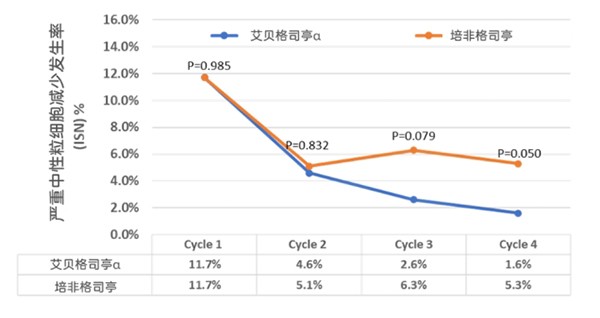
各化療周期的4級中性粒細胞減少發生率
在安全性方面,兩組的不良事件發生率相似,最常見的不良事件為骨痛、惡心和乏力,艾貝格司亭α組的骨痛均為輕度至中度。除了來自于化療方案的不良事件(例如惡心、嘔吐、腹瀉、脫發、疲勞等),本研究未報告與藥物相關的嚴重不良事件[1]。
參考文獻:
[1]John A. Glaspy, Igor Bondarenko, Sergei Tjulandin, et al. Efbemalenograstim Alfa, a Long-Acting Granulocyte Colony-Stimulating Factor Fusion Protein Without PEGylation, Versus Pegfilgrastim for Management of Chemotherapy-Induced Neutropenia in Patients With Breast Cancer: Results of a Phase III Randomized Noninferiority Trial. 2, e2400074(2025).
[2]Qingyuan Zhang, Zhonghua Wang, et al. A randomized, multicenter phase III Study of once-per-cycle administration of efbemalenograstim alfa (F-627), a novel long-acting rhG-CSF, for prophylaxis of chemotherapy-induced neutropenia in patients with breast cancerl[J]. BMC Cancer, (2024) 24:1143.
[3]Glaspy J, Bondarenko I, Burdaeva O, et al. Efbemalenograstim alfa, an Fc fusion protein, long-acting granulocyte-colony stimulating factor for reducing the risk of febrile neutropenia following chemotherapy: results of a phase III trial[J]. Supportive Care in Cancer, (2024) 32:34.
聲明:
1.新聞稿旨在促進醫藥信息的溝通和交流,僅供醫療衛生專業人士參閱,非廣告用途。
2.本公司不對任何藥品和/或適應癥作推薦。
3.本新聞稿中涉及的信息僅供參考,不能以任何方式取代專業的醫療指導,也不應被視為診療建議。若您想了解具體疾病診療信息,請遵從醫生或其他醫療衛生專業人士的意見或指導。
 簡體中文
簡體中文 English
English















